【研究背景】
目前,為了開發高安全性和高能量密度的下一代鋰離子電池,具有固態電解質(石榴石型、NASICONs、硫化物和鈣鈦礦等)的全固態電池(ASSBs)受到研究人員的廣泛關注。其中,固態硫化物電解質(S-SEs)基ASSBs具有優異的Li+離子傳導率,在室溫下可以達到1.7×10−2 S cm−1(Li7P3S11),接近於有機電解質。然而,S-SEs也面臨著巨大的挑戰,首先,S-SEs基電池中的固固介面阻抗過大,且在充放電過程中有體積膨脹現象,從而可能導致粉化和破裂;另外,S-SEs是不穩定的,其暴露在空氣中容易發生水解產生H2S氣體,影響電化學效能。同時,為了能大規模製備柔性的片狀S-SEs基電極,研究人員大多采用加入溶劑、粘結劑和導電劑與S-SEs混合的溼法制備工藝,但大多數用於溶解粘結劑的有機溶劑的極性官能團會與S-SEs發生反應,因此,溶劑和粘結劑與S-SEs的相容性問題使得漿料製備過程非常困難。目前,針對S-SEs在溼空氣中的化學穩定性以及與溶劑或粘結劑的相容性問題並沒有詳細的總結。
圖1.(a)S-SEs的優勢和挑戰和(b)S-SEs的化學相容性問題。
有鑑於此,國立臺灣科技大學的Wei-Nien Su和Bing Joe Hwang等人系統地綜述了S-SEs的化學穩定性的基本原理、表徵技術和設計策略。在第二章節,作者對S-SEs與溼空氣、溶劑和粘結劑的化學穩定性之間的原理進行探究,隨後在第三章節討論了一些改善S-SEs化學穩定性的策略,並在最後一章節進行了總結和展望。
【綜述亮點】
1. 全面介紹了S-SEs作為鋰離子電池電解質的優勢以及存在的挑戰;
2. 為了今後實現大規模S-SEs基電極製備,系統地總結了S-SEs與溶劑、聚合物粘結劑均勻混合的化學相容性問題;
3. 探討了提高S-SEs穩定性和相容性的策略,旨在解決S-SEs基ASSBs在實際應用中面臨的基礎科學問題。
【內容簡介】
1. S-SEs的化學穩定性
將化學不穩定的S-SEs引入到ASSBs會極大地影響電池的效能並降低能量密度。材料的化學穩定性可以調節電池元件以及生產工藝和條件。
1.1 S-SEs對溼空氣的化學穩定性
S-SEs暴露於溼空氣中會與水反應生成有毒的H2S,從而導致其晶體結構發生改變,極大地影響材料的離子傳導率,降低電化學效能。以Li7P3S11為例,P2S74−陰離子是主要單元,其與H2O反應先形成OH和SH,隨後SH與H2O反應形成OH和H2S。
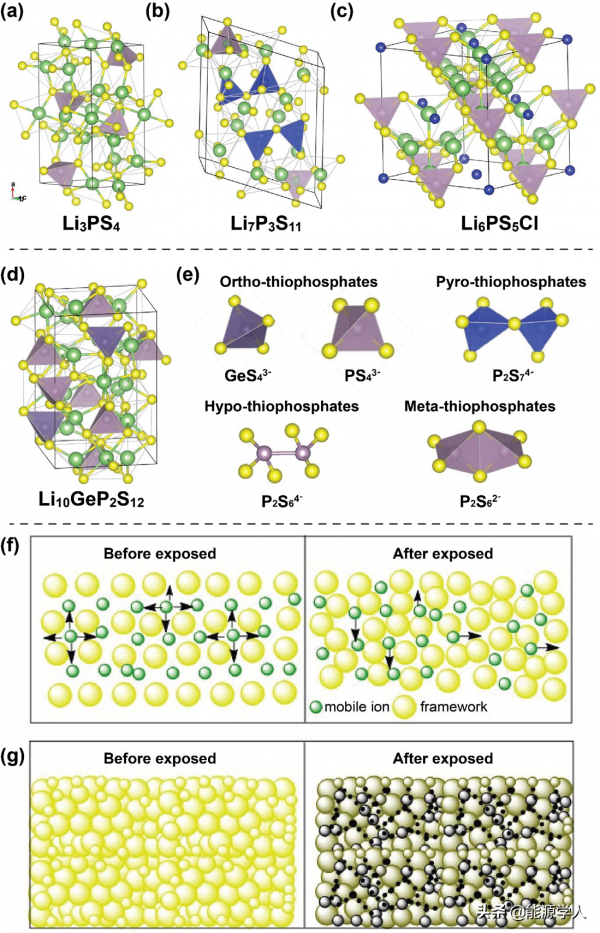
圖2.(a-d)不同型別的S-SEs晶體結構,(e)不同型別的硫代磷酸鹽,S-SEs在暴露於空氣或極性溶劑前後的(f)離子遷移率和(g)微結構變化示意圖。
1.2 S-SEs與溶劑和粘結劑的化學相容性
為了實現大規模的S-SEs製備,通常採用含有粘結劑的漿料工藝以使各組分緊密接觸,而此時SEs在溶劑中的穩定性就顯得尤其重要,對於S-SEs,只能使用非極性的溶劑/粘結劑進行製備,如目前已經報道的Li6PS5Cl/Li3PS4與聚合物粘結劑丙烯腈丁二烯和PVP,然而,S-SEs如何與溶劑/粘結劑中不同官能團的相互作用仍不明確,更好地認知S-SEs的相容性可以幫助選擇合適的溶劑和粘結劑,從而成功地使用漿料工藝(S-SEs不溶解)。
1.2.1 與溶劑的相容性
高極性的溶劑通常是強的Lewis鹼,包含有帶孤對電子的N和O等電負性元素,基於強弱酸鹼(HSAB)法則,N和O容易與S-SEs中的親電物種(如P5+)進行反應,另外,S-SEs硫代磷酸鹽(P2S74−和PS43−)中的S原子可能會攻擊羰基中的親電C原子,由於S-SEs與極性溶劑的相互作用,從而生成低離子傳導率的相。因此,在一些非極性溶劑中,S-SEs可以保持穩定,包括甲苯,二甲苯和四氫呋喃。
圖3.(a)不同極性程度溶劑與S-SEs相容性和(b)可能的溶劑親核攻擊S-SEs示意圖。
1.2.2 與粘結劑的相容性
漿料法制備電極中需要粘結劑的存在以讓各組分更緊密的結合,減少顆粒間的阻抗,傳統的粘結劑包括羧甲基纖維素(CMC)、聚乙烯醇(PVA)和聚(偏二氟乙烯)(PVDF)具有較強的結合能力,但其存在極性官能團,也需要極性較強的溶劑,從而粘結劑、溶劑和S-SEs三者之間需要得到一個平衡。
圖5. S-SEs與溶劑相容性的示意圖。其中,SEBS:苯乙烯乙烯丁烯苯乙烯共聚物,SBR:苯乙烯丁二烯橡膠,BR:丁二烯橡膠,PTFE:聚四氟乙烯,PIB:聚異丁烯,NBR:丁腈橡膠,PVB:聚乙烯醇丁醛,PVA:聚乙烯醇乙酸酯,THF:四氫呋喃,PMMA:聚甲基丙烯酸甲酯,PET:聚對苯二甲酸乙二醇酯,PVdF:聚偏氟乙烯,CMC:羧甲基纖維素,PAN:聚丙烯腈,NMP:N-甲基吡咯烷酮,PC:碳酸丙烯酯。
1.3 表徵技術
理解S-SEs的不穩定行為有利於構建安全和高活性的電解質,大多數的研究關注於S-SEs的晶體結構、微結構、機械效能和離子傳導率的變化來判斷不穩定性,也可以研究H2S的釋放,另外就是結合理論去預測S-SEs的化學穩定性。
1.3.1 顏色變化
圖6. Li7P3S11在不同溶劑中顏色變化研究。
1.3.2 晶體結構分析
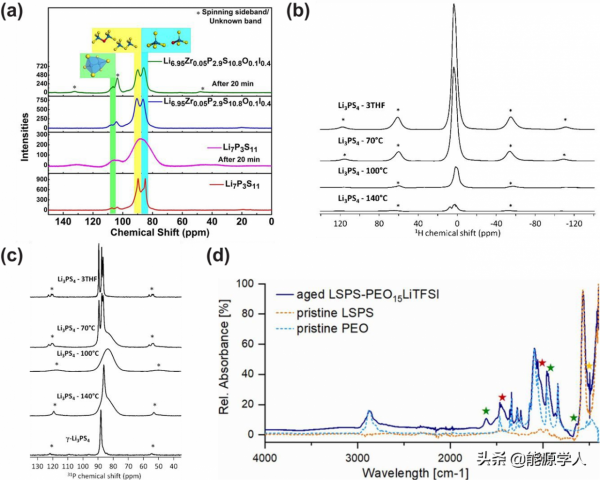
圖8.(a)藉助非原位31P魔角旋轉核磁共振(MAS-NMR)檢測Li7P3S11和Li6.95Zr0.05P2.9S10.8O0.1I0.4的化學穩定性和區域性結構分析,(b)不同溫度處理的Li3PS4玻璃的質子MAS波譜,(c)相同Li3PS4玻璃的31P MAS波譜,星號代表自旋邊帶,(d)老化的LSPS|PEO-LiTFSI(LSPS為Li10SnP2S12,PEO為聚環氧乙烷,LiTFSI為雙三氟甲基磺酸亞醯胺鋰)混合物與原始LSPS的傅立葉紅外光譜(FTIR)對比。
1.3.3 微結構和表面組分分析
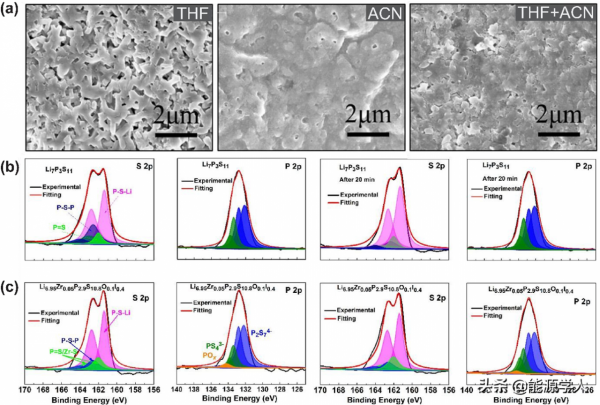
圖9. 用乙腈(ACN),四氫呋喃(THF)以及ACN和THF混合溶液製備的Li7P3S11微球SEM圖,暴露於溼空氣前後的S 2p和P 2p XPS光譜:(b)Li7P3S11,(c)Li6.95Zr0.05P2.9S10.8O0.1I0.4。
1.3.4 離子傳導率分析
圖10.(a)由THF,ACN以及其混合溶液製備得到的Li7P3S11微球的EIS奈奎斯特曲線,(b)Li7P3S11暴露溶劑後的離子電導率(σSE’)(扣除原始Li7P3S11的σSE)作為溶劑孤對電子供體數量的函式(親核性與孤對電子供體數量呈正相關)。
1.3.5 重量分析和H2S氣體檢測
圖11.(a)純O2下LPSI和LPSI-20Sn電解質的時間分辨質量變化,空氣中S-SEs水解生成的H2S氣體測量的(b)常規裝置和(c)設計裝置。
1.3.6 機械效能
表徵S-SEs在溼空氣或漿料工藝中進行機械穩定性有助於大規模製備,基於漿料工藝製備的S-SEs可以既具有高度的緻密性又具有良好的柔韌性,但聚合物粘結劑的極性特徵對機械穩定性有較大的影響。
1.3.7 理論分析
通常可以理論計算S-SEs與H2O反應生成H2S的焓變(ΔE)來判斷熱動力學相關的反應過程,一個負的ΔE意味著熱力學反應可以進行,說明S-SEs在該體系下不穩定。
2. 改善S-SEs化學穩定性的策略
2.1 S-SE和溼空氣
2.1.1. 使用新增劑
1)氧化物新增劑
氧化物與H2S的反應過程是自發進行的(MxOy+H2S→MxSy+H2O),因此可以在S-SEs中新增氧化物吸收H2S,從而提高S-SEs在溼空氣下的穩定性。
2)沸石新增劑
沸石由於具有3 D的多孔結構,其可以作為分子篩去吸收H2O和H2S,從而避免S-SEs發生不利的副反應。
3)鹵化鋰新增劑
4)金屬硫化物新增劑
研究表明,硫化物(如FeS)可以作為催化劑有效的將H2S轉變為S晶體。
圖12.(a)H2S生成量與暴露在空氣中時間的關係,(b)90Li3PS4-10MxOy(MxOy:ZnO,Fe2O3和Bi2O3)複合材料和Li3PS4玻璃的氣相色譜圖,(c)沸石作為新增劑防止S-SE接觸溼空氣示意圖(c)純的Li6PS5Cl,(d)沸石嵌入Li6PS5Cl,(e)加入LiI前後的Li3PS4化學穩定性比較,(f)DFT計算的Li4PS4I和Li3PS4與水反應的能量(0 K)。
2.1.2. 應用HABS法則
根據HABS法則,O2−(高電負性)的鹼性比S2−,從而更易與強酸P5+進行反應。
1)陽離子摻雜
減少S-SEs中P的含量可以避免P-O的形成,從而提高S-SEs在溼空氣中的穩定性,因此採用其它陽離子取代P5+是可行的。
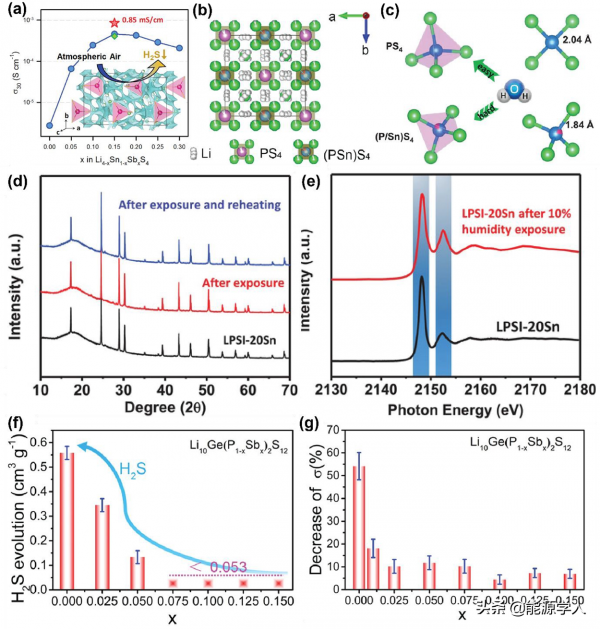
圖13.摻雜Sb的Li4SnS4 S-SE在空氣中具有較高的穩定性和離子導電性,(b)製備的LPSI-20Sn(Li6.24P0.823Sn0.177S4.58I0.9)的結構(垂直於c軸的角度),(c)基於DFT計算的PS4和(P/Sn)S4四面體被水氧化難易程度示意圖,(d)LPSI-20Sn以及10%溼度下暴露後的XRD譜圖和(e)P k邊X射線吸收近邊結構(XANES),(f)商業的Li10GeP2S12和合成的Li10Ge(P1−xSbx)2S12 S-SE粉體產生的H2S氣體量,(g)Li10Ge(P1−xSbx)2S12(0≤x≤15%)S-SEs暴露於空氣後離子電導率下降。
2)用O2−部分取代S-SE中的S2−
相比於S2−,O2−與P5+鍵合能力更強,從而可以考慮用O2−部分取代S-SE中的S2−。
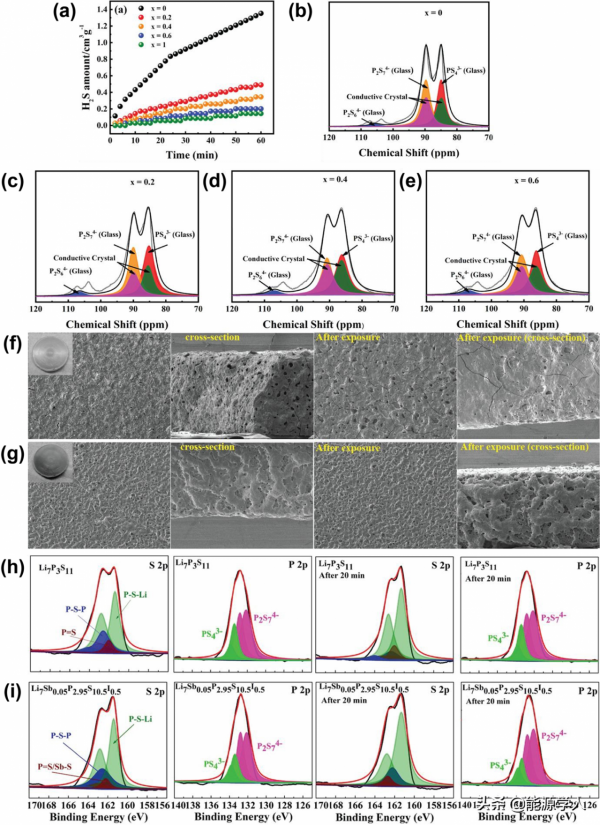
圖15.(a)Li7−0.06(x)P3−0.03(x)NbxS11−0.11(x)O3x S-SEs暴露在潮溼空氣中60 min的H2S氣體釋放量,(b)Li7−0.06(x)P3−0.03(x)NbxS11−0.11(x)O3x S-SEs S-SEs的31P MAS-NMR譜圖分峰(注:在x≥0.2,導電晶體的峰P2S74−(粉紅色)和PS43−(綠色)分別代表(P2S74−+P2OS64−)和(PS43−+POS33−)),(f)Li7P3S11和(g)Li7Sb0.05P2.95S10.5I0.5微球接觸空氣前後的表面和截面SEM影象,(h)Li7P3S11和(i)Li7Sb0.05P2.95S10.5I0.5暴露於空氣20分鐘前後的S 2p和P 2p 的XPS譜圖。
2.1.3 核殼設計
為避免S-SEs與溼空氣反應,可以考慮在電解質表明設計一層奈米包覆層的核殼奈米結構,可以透過調節殼的組分來改善S-SEs的穩定性。
圖16.(a)製備純淨的和氧化硫化物包覆的Li6PS5Cl粉末的工藝示意圖,(b)純的和核殼結構的SE顆粒之間的空氣穩定性和化學脆弱性示意圖,(c)SE在25 ℃,相對溼度為35%的空氣中放置120分鐘的離子電導率的變化,純的Li7P3S11 S-SE和具有疏水SEBS聚合物的複合材料的(d)H2S氣體的釋放量隨不同空氣暴露時間的變化以及(e)在水浸泡前後的圖片。
2.1.4 合成方法
圖17.(a)傳統的固相法和一步氣相法合成過程比較,(b)LSPSC,LPS,LSS和LSAS總的H2S生成量隨時間變化的關係,(c)純的,水浸泡後和水浸泡500 ℃熱處理後LSPSC,LPS和LSAS的拉曼光譜。
2.2 S-SEs與溶劑
2.2.1 應用低極性溶劑
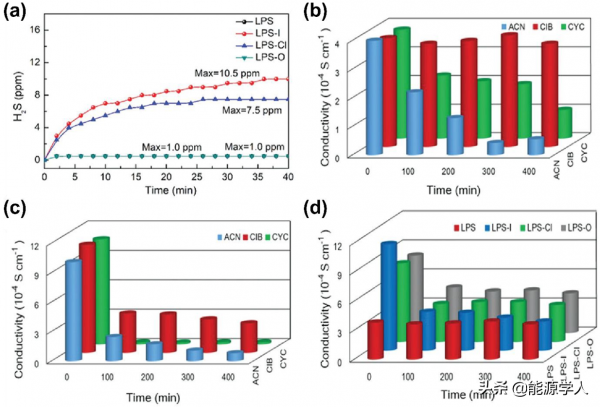
圖18. S-SEs在有機溶劑和潮溼空氣中的化學穩定性。
2.2.2使用溶劑化離子液體
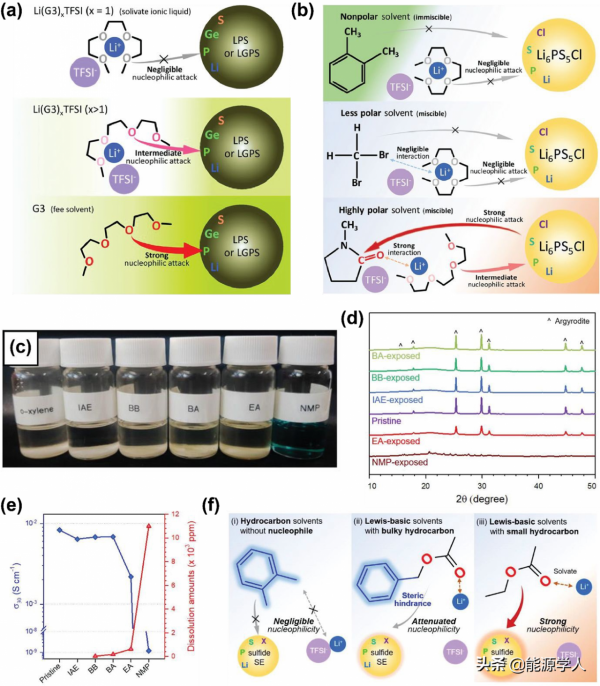
圖20.(a)乙二醇二甲醚基溶劑(三乙二醇二甲醚(G3)和Li(G3)xTFSI))與LPS和LGPS S-SEs反應的示意圖,(b)不同極性溶劑稀釋的LiG3(Li(G3)TFSI)與Li6PS5Cl反應性示意圖,不同溶劑與LPSX S-SE混合的光學照片(c),混合物的XRD圖譜(d),Li+傳導率和稀釋量(e);(f)LPSX S-SE與不同型別的溶劑反應示意圖(Ⅰ):烷烴溶劑,(Ⅱ):大分子烷烴Lewis鹼溶劑(Ⅲ):小分子烷烴Lewis鹼溶劑。
2.3 S-SEs與粘結劑
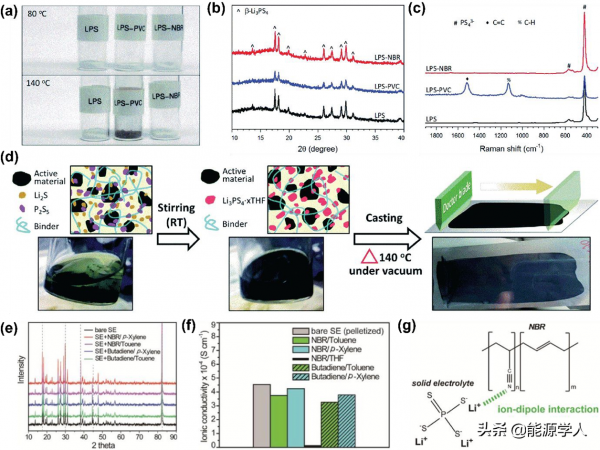
圖21. 溼化學法制備的S-SE-粘結劑複合材料的表徵。(a)S-SE聚合物粘結劑複合材料在不同溫度下熱處理後的照片,(b)XRD譜圖,(c)Raman譜圖,(d)單步溼化學法制備複合電極的示意圖,(e)S-SE在丁腈橡膠和聚丁二烯粘結劑溶液中浸泡24 h後的XRD譜圖,(f)浸泡在粘結劑溶液中的S-SE的鋰離子電導率,(g)S-SE與NBR粘結劑的分子間相互作用。
【總結與展望】
總之,本文系統的總結了S-SEs對溼空氣的化學穩定性以及與溶劑和粘結劑的相容性問題,從S-SEs化學穩定性的基礎理解、表徵技術到S-SEs化學穩定性的改善策略進行了詳盡的討論,主要有以下幾點:
1)S-SEs與溶劑的相容性問題:S-SEs對強極性溶劑非常敏感,這些溶劑中含有孤立電子對會與S-SE中的P物種發生反應,從而導致S-SEs結構發生改變,
2)S-SEs與粘結劑的相容性問題:根據相似相溶原理,非極性粘結劑需要與非極性溶劑相溶,但非極性粘結劑缺乏給予孤對電子的原子,從而不能保證足夠的粘結性,可以採用原位去保護方法避免S-SEs與聚合物粘結劑反應或使用非粘結劑策略;
3)S-SEs對溼空氣的穩定性:S-SEs在溼空氣中會與H2O發生反應生成H2S,可以採用吸附劑(如金屬氧化物ZnO、硫化物FeS和鹵化鋰LiI)與H2S反應進行去除,利用HABS法則進行陽離子取代和陰離子摻雜或設計核殼結構保護S-SEs等。
目前雖有不少方法用來解決S-SEs穩定性和相容性問題,但這些策略仍存在S-SEs離子傳導率低且仍不然在溼空氣下保持長期的穩定,為實現S-SEs基ASSBs,有關S-SEs的幾個關鍵性問題亟需解決:
1)提高粘結劑對介面阻抗的影響:應合理調節S-SEs、活性材料和粘結劑之間的三相介面以保證有效的離子傳導率;
2)提高粘結劑在S-SEs基ASSBs中的粘結性:為了獲得長迴圈壽命和高比容量的ASSBs,粘結劑需要與溶劑和S-SEs均勻混合並實現緊密連線,同時要避免粘結劑和S-SEs發生反應;
3)提高S-SEs在空氣下的穩定性:在S-SEs中P作為酸而S作為鹼,S具有孤對電子,從而可以使用Lewis酸吸附新增劑對S-SE表面進行處理產生Lewis酸鹼相互作用,其可以避免電解質與溼空氣發生反應,另外也可以設計無P5+價的S-SEs也可以構建化學穩定的結構;
4)標準測試方案:需要建立一個標準和統一的H2S測試方案,S-SEs反應量、測試腔體的體積、溫度、相對溼度、溫度等均需要考慮;
5)深入理解S-SEs反應:需要開發先進的分析技術用來理解在漿料製備過程中S-SES和水汽、溶劑和粘結劑的相互作用;
6)成本:目前大部分關於S-SEs不穩定的解決方案是成本高昂的,為此需要進一步關注大規模製備ASSBs所需的成本;
7)S-SEs與溼空氣或漿料工藝中化學反應的溫度依賴動力學仍是一個尚未深入研究的開放領域。
Yosef Nikodimos, Chen-Jui Huang, Bereket Woldegbreal Taklu, Wei-Nien Su*, Bing Joe Hwang*, Chemical Stability of Sulfide Solid-state Electrolytes: Stability Toward Humid Air and Compatibility with Solvents and Binders, Energy Environ. Sci., 2022, DOI:10.1039/D1EE03032A