近期主要科研成果
中山醫院放療科揭示放療聯合免疫治療新機制
1月2日,復旦大學附屬中山醫院放療科發文揭示放療聯合免疫治療新機制,研究結果線上發表在著名的國際放射腫瘤學雜誌(International Journal of Radiation Oncology Biology Physics ),此雜誌由美國放射治療及腫瘤學會(ASTRO)主辦,是放射治療專科的最具影響力期刊之一。
前期大量的臨床研究已經證明放療聯合免疫可達到珠聯璧合的協同增效作用,已成為腫瘤全新的治療模式寫入指南。但放療聯合免疫治療內在機制仍然不明確,既往的研究認為區域性放療促進腫瘤相關抗原釋放,主要組織相容性複合物(MHC I)分子表達及免疫細胞招募產生一種系統的、 免疫介導的全身抗腫瘤反應,本研究從全新的視角闡述了放療聯合免疫治療協同增效機制。
劉曉慧博士等報道利用臨床蛋白質組技術助力顱內動脈瘤血清標誌物鑑定及相關發病機理表徵
1月3日,生物醫學研究院劉曉慧博士聯合華山醫院冷冰主任醫生在EMBO Molecular Medicine雜誌上線上發表一篇題為“Circulating proteomic panels for risk stratification of intracranial aneurysm and its rupture”的論文,透過建立基於質譜的全面血清標誌物篩選方法,揭示了可能存在的顱內動脈瘤臨床血清標誌物以及疾病發生髮展可能的機制。
王永輝團隊與華東理工大學黃瑾團隊聯合在RORγt/DHODH雙靶點抑制劑方面取得進展
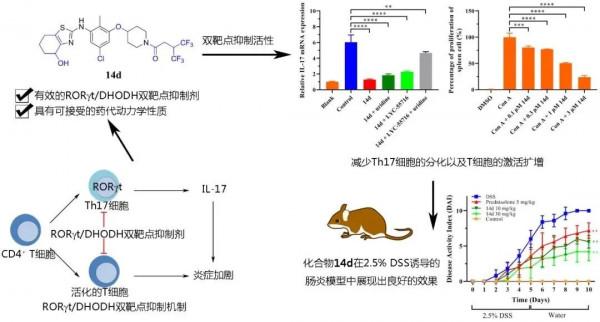
近日,復旦大學藥學院藥物化學系王永輝研究員團隊與華東理工大學藥學院黃瑾教授團隊合作,在藥物化學領域權威期刊Journal of Medicinal Chemistry上發表了題為“Discovery of Orally Available Retinoic Acid Receptor-Related Orphan Receptor γ-t/Dihydroorotate Dehydrogenase Dual Inhibitors for the Treatment of Refractory Inflammatory Bowel Disease”的研究論文,併入選期刊封面文章。該論文提出RORγt/DHODH雙靶點抑制劑的炎性腸病(inflammatory bowel disease, IBD)治療新策略,發現一類具有四氫苯並噻唑母核的RORγt/DHODH雙靶點抑制劑,在體內外模型中顯示出良好的抗炎性腸病活性。
王建新課題組在腫瘤免疫化療聯合治療領域取得進展
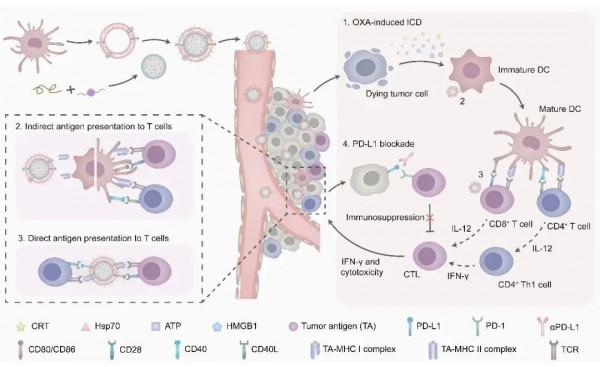
近日,國際知名學術期刊《生物活性材料》(Bioactive Materials)線上發表了復旦大學藥學院王建新教授團隊題為《用於免疫原性化療和腫瘤抗原特異性免疫治療的載奧沙利鉑奈米粒成熟樹突狀細胞衍生囊泡》(Mature dendritic cell-derived dendrosomes swallow oxaliplatin-loaded nanoparticles to boost immunogenic chemotherapy and tumor antigen-specific immunotherapy)的研究成果。該論文報道了一種樹突狀細胞(DC)仿生納米制劑,可參與免疫化療聯合療法,放大腫瘤免疫應答效應,具有顯著的抗腫瘤效果。
黃志力課題組發現調控覺醒新核團
黃志力課題組發現背側紋狀體多巴胺D1受體(Dopamine D1 receptor,D1R)陽性神經元參與覺醒的啟動和維持。北京時間2022年1月12日凌晨0時,相關研究成果以《紋狀體多巴胺D1受體陽性神經元促進小鼠覺醒》(Striatal neurons expressing dopamine D1 receptor promote wakefulness in mice)為題,線上發表於Current Biology。
研究團隊利用光遺傳學、化學遺傳學、光纖鈣訊號測定神經元活性和腦電/肌電記錄等方法研究了背側紋狀體D1R神經元調控睡眠覺醒的作用及神經環路。結果發現光遺傳學啟用背側紋狀體D1R神經元誘導小鼠從非快眼動 (non-rapid eye movement,NREM) 睡眠到覺醒的快速轉變,而抑制紋狀體 D1R 神經元活性,顯著減少小鼠覺醒時長。結果提示紋狀體D1R 神經元參與調控覺醒。
李聰教授團隊搭建定位“代謝邊界”的腦膠質瘤手術導航系統
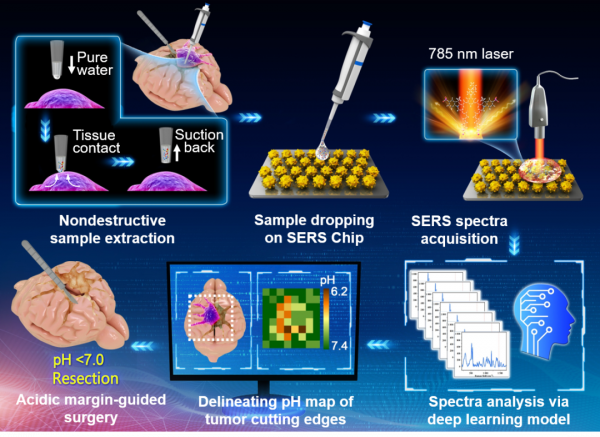
近日,復旦大學藥學院李聰教授、類腦智慧科學與技術研究院張孝勇研究員、資訊科學與技術學院餘錦華教授以及附屬華山醫院神經外科毛穎教授聯合研究團隊構建了一類基於表面增強拉曼散射(SERS)技術的膠質瘤手術導航原理驗證系統。該工作以《智慧拉曼導航系統術中劃定酸化區域引導腦腫瘤切除》(Intelligent SERS Navigation System Guiding Brain Tumor Surgery by Intraoperatively Delineating the Metabolic Acidosis)為題線上發表於《先進科學》(Advanced Science)雜誌。該系統由自主研製的pH響應SERS晶片,手持式拉曼光譜儀以及拉曼光譜深度學習系統組成。該工作提出了水滴輔助組織取樣技術,能夠將手術切面可疑組織表面代謝物無損地轉移到SERS晶片上。還提出了報告分子誘導表面增強拉曼共振效應新原理。實現了微量液滴樣本pH值的快速測定。自主構建的深度學習模型自動分析樣本拉曼光譜並準確、快速地測定樣品pH值。該智慧SERS系統導航可在6分鐘內對64個組織位點(約1 cm2)pH進行測量,並透過繪製組織pH分佈圖定位“酸性代謝邊界”。與臨床手術導航技術相比,基於“酸化邊界”的手術導航策略顯著提高大鼠膠質瘤模型存活率,延緩了腫瘤復發速度。此外,透過5例病人膠質瘤組織樣本分析,也發現了酸化與惡性程度之間的相關性,揭示了“代謝邊界”手術導航策略臨床轉化的可行性。
胡晉川團隊等與合作者報道單鹼基解析度水平上的DNA脫氧尿嘧啶的檢測技術
1月17日,生物醫學研究院胡晉川研究員、錢茂祥研究員與同濟大學陳義漢院士、馬紅輝研究員合作在國際權威刊物《美國化學會志》(Journal of the American Chemical Society)上發表了題為“基於UdgX的在單鹼基解析度水平上的DNA脫氧尿嘧啶的檢測技術”的研究論文。藉助被稱之為UdgX的特殊的酶分子,該研究發明了靈敏性好、特異性強和解析度高的DNA脫氧尿嘧啶(dU)檢測技術,第一次用酶法在單鹼基解析度水平上精準檢測DNA中的dU,實現了DNA中dU鹼基檢測技術的根本性突破。
陸路/姜世勃/袁正宏團隊聯合多家單位開發基於新型佐劑的β屬冠狀病毒B譜系候選通用疫苗
1月19日復旦大學基礎醫學院陸路/姜世勃/袁正宏團隊聯合多家單位在Cell Research雜誌線上發表了題為“A novel STING Agonist-Adjuvanted Pan-Sarbecovirus Vaccine Elicits Potent and Durable Neutralizing Antibody and T Cell Responses in Mice, Rabbits and NHPs”的研究論文,報道了一種基於新型非核苷酸類STING小分子激動劑為佐劑,以最原始的新冠病毒刺突(S)蛋白受體結合域(RBD)偶聯的人IgG Fc片段(RBD-Fc)為抗原而構建的一個β-CoV-B(Sarbecovirus)通用疫苗。該疫苗可在多種動物模型(包括小鼠、兔以及恆河猴)誘匯出針對SARS-CoV-2、SARS-CoV-2變異株、SARS-CoV以及來自於蝙蝠的SARSr-CoV的廣譜、強效、長效的體液和細胞免疫應答。從而,提出了一種應對新發病毒大流行的疫苗研發策略:在新發病毒首次出現後,基於新型佐劑輔以第一代原始病毒抗原,開發出對未來出現的變異株及同類相關病毒新變種,均有高效保護潛力的廣譜疫苗。該“以不變應萬變”的策略為解決新發病毒變異對疫苗研發提出的挑戰提供了新思路。
陳舌研究員/王碧芸教授/付朝偉教授團隊發現預測鉑類化療敏感性的新型液體活檢標誌物
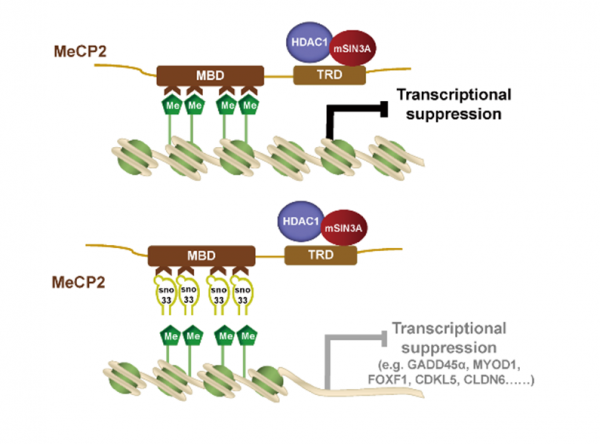
復旦大學基礎醫學院陳舌研究員、附屬腫瘤醫院王碧芸教授及公共衛生學院付朝偉教授團隊合作發現血漿小核仁RNA SNORD33對於三陰性乳腺癌患者鉑類藥物敏感性的預測作用,並揭示甲基化結合蛋白MeCP2參與SNORD33調控的鉑類耐藥分子機制。相關研究成果A plasma SNORD33 signature predicts platinum benefit in metastatic triple-negative breast cancer patients近日線上發表於Molecular Cancer期刊上。本研究結果提供了高準確性、檢測便利、非侵入性的新的分子標記物和治療的特異性靶標。採集0.2毫升血漿檢測SNORD33水平,結合臨床特徵,即可實現預測轉移性三陰性乳腺癌鉑類藥物療效,為腫瘤患者帶來更多獲益。在新輔助化療及其它癌種患者含鉑治療方案中的應用,相關驗證工作正在有序開展中。
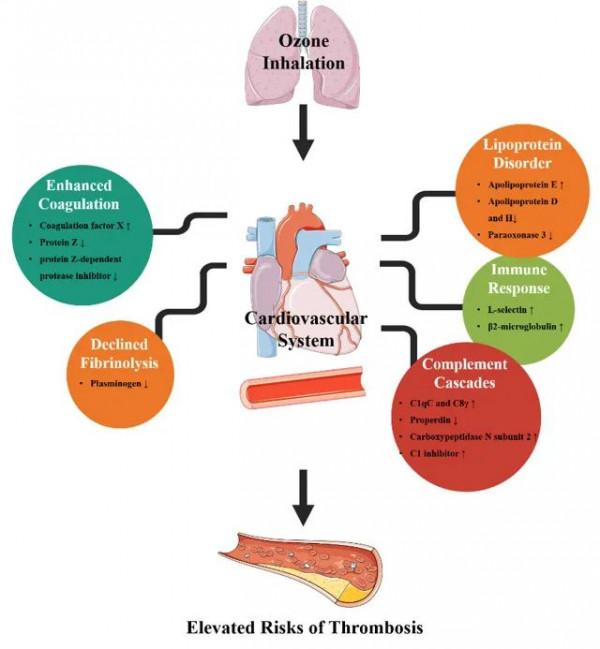
闞海東與陳仁杰課題組蛋白組學研究揭示臭氧暴露或可引起機體凝血狀態改變
復旦大學公共衛生學院闞海東與陳仁杰課題組,透過一項隨機交叉對照研究,發現臭氧短期暴露對凝血/纖溶系統、脂蛋白代謝、免疫/補體系統產生影響,研究結果以“Ozone exposure and prothrombosis: Mechanistic insights from a randomized controlled exposure trial”為題發表在Journal of Hazardous Materials 雜誌上。本研究利用非靶向蛋白組學技術,初步探索了臭氧暴露引起的蛋白特徵譜改變,研究結果為臭氧誘發的血栓形成提供了合理的分子生物學解釋,為未來開展深入的分子機制研究積累了豐富的蛋白組資料。
葉丹團隊揭示CEBPA是DNMT3A的特異性抑制因子
1月26日,生物醫學研究院和華山醫院雙聘教授葉丹團隊在Science Advances上發表題為“Tumor suppressor CEBPA interacts with and inhibits DNMT3A activity”的研究成果,首次報道了CEBPA是DNMT3A的特異性抑制因子。該工作首次報道了CEBPA是DNMT3A的特異性抑制因子,揭示了在基因組特定區域DNMT3A調控新機理,併為攜帶CEBPA突變的白血病患者臨床治療提供了潛在方案。
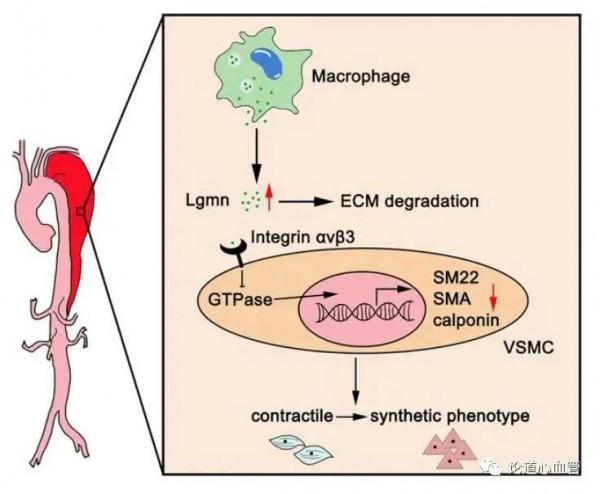
葛均波院士/孫愛軍教授團隊揭示Lgmn介導的平滑肌細胞表型轉化促進主動脈夾層進展
1月31日,來自復旦大學附屬中山醫院的葛均波院士與孫愛軍教授團隊在Circulation上發表了題為“Legumain Is an Endogenous Modulator of Integrin αvβ3 Triggering Vascular Degeneration, Dissection, and Rupture”的文章,探討了Legumain(Lgmn)介導的平滑肌細胞表型轉化調控主動脈夾層的作用機制。該文章證實了Lgmn在TAD發病過程中的重要作用。在TAD發病程序中,Lgmn表達增加,並伴有ECM降解和血管平滑肌表型轉化。巨噬細胞來源的Lgmn結合並阻斷VSMCs中的Integrin αvβ3通路,導致Rho GTPase受到抑制,從而破壞VSMCs分化相關基因的轉錄,誘導VSMCs表型轉化、血管變性與TAD進展。文章指出,敲除或者抑制Lgmn可能是一種很有前途的治療TAD的新策略。
來源:復旦上醫(各院系、附屬醫院)
責編:章佩林
編輯:徐俊奕