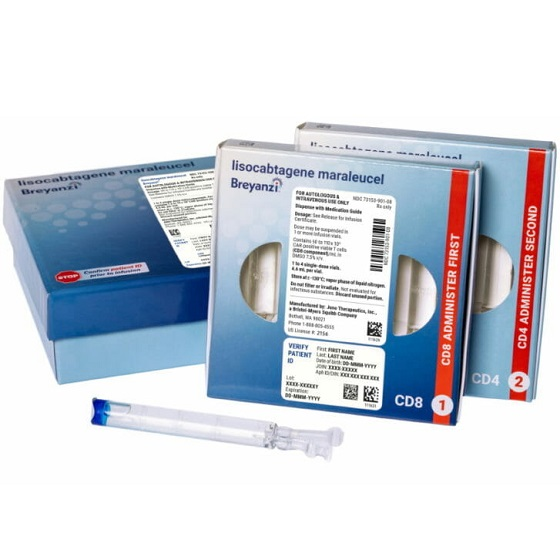
2022年2月17日,美國FDA已授予靶向CD19的CAR-T細胞療法Breyanzi(lisocabtagene maraleucel)的補充生物製品許可申請(sBLA)優先審評資格,用於一線治療失敗後的復發/難治性大B細胞淋巴瘤(LBCL)成人患者。
Breyanzi是一種自體、CD19導向、嵌合抗原受體(CAR)T細胞療法,具有明確的組成和4-1BB共刺激域。2021年2月,美FDA批准Breyanzi上市用於治療兩種或兩種以上全身治療的復發或難治性的大B細胞淋巴瘤成人患者。
商品名:Breyanzi
通用名:lisocabtagene maraleucel(liso-cel)
美國首次獲批:2021年2月
中國首次獲批:未獲批
獲批適應症:復發/難治性大B細胞淋巴瘤(LBCL)
臨床資料
此次優先審查的授予是基於一項全球性、多中心、隨機的III期TRANSFORM試驗(NCT03575351)的資料,主要評估了CD19 CAR-T細胞療法Breyanzi與與目前標準治療(標準挽救性化療+大劑量化療+自體造血幹細胞移植)在復發或難治性大B細胞淋巴瘤成人患者中的療效和安全性。
試驗的主要終點是無事件生存期(EFS);關鍵的次要終點包括完全緩解(CR)率、無進展生存期(PFS)和總生存期(OS),其他次要的終點包括持續緩解時間(DOR)、客觀緩解率(ORR)和安全性。
當中位隨訪時間為6.2個月時,Breyanzi治療組(n=92) VS 標準治療組(n=92)的中位EFS為10.1個月 VS 2.3個月,6個月的EFS率為63.3% VS 33.4%,12個月的EFS率為44.5% VS 23.7%;中位PFS為14.8個月 VS 5.7個月,6個月PFS率為69.4% VS 47.8%,12個月PFS率為52.3% VS 33.9%。此外,兩組的CR率為66% VS 39%;ORR為86% VS 48%。
OS資料在資料截止時還不成熟,但觀察到一個有利於CAR-T細胞治療的數值趨勢。Breyanzi治療組 VS 標準治療組的中位OS為尚未達到(NR) VS 16.4個月;6個月的OS率為91.8% VS 89.4%;12個月OS率為79.1% VS 64.2%。
不良反應
所有接受Breyanzi治療的患者報告了治療緊急不良反應(TEAEs),而99%接受標準治療的患者報告了治療緊急不良反應。Breyanzi治療組最常見的不良反應包括:中性粒細胞減少(82%)、貧血(63%)和血小板減少(58%)。
92%接受Breyanzi治療的患者經歷了3級或更高的不良反應,而在接受標準治療患者中該比例為87%。在接受Breyanzi治療的患者中,常見的3級或更高級別的不良反應包括:中性粒細胞減少(80%)、貧血(49%)、血小板減少(49%)和淋巴細胞減少(25%)。
結論
該試驗發現,與標準治療相比,Breyanzi能顯著改善無事件生存時間、完全緩解率、無進展生存期。這說明,在復發或難治性LBCL患者中,Breyanzi有潛力成為一線治療失敗後患者的新護理標準。
參考來源:
https://www.onclive.com
【重要提示】本公號【全球好藥資訊】所有文章資訊僅供參考,具體治療謹遵醫囑!