撰文 | YQ
責編 | 翊竑
急性髓系白血病(AML)是由於造血幹細胞分化障礙及增殖過度所致異常骨髓造血前體細胞聚集的造血幹細胞惡性克隆性疾病。AML在成人白血病中較為常見,通常致死率也較高。近年研究表明,表觀遺傳異常是導致造血幹細胞分化障礙的主要原因之一,因此,研究AML的表觀遺傳調控機制,對於理解AML的發病機理、尋找新的治療靶標和開發新的針對AML的治療方法都具有重要的意義。
近日,來自賓夕法尼亞大學獸醫學院的M. Andrés Blanco課題組與來自麻省總醫院的David B. Sykes課題組,在Cancer Discovery上發表了題為KAT6A and ENL form an epigenetic transcriptional control module to drive critical leukemogenic gene expression programs的文章,該文章透過CRISPR篩選的方式,發現了KAT6A可以透過表觀遺傳調控AML關鍵基因的表達,從而促進AML的發生,抑制KAT6A活性可以作為潛在的AML治療藥物。
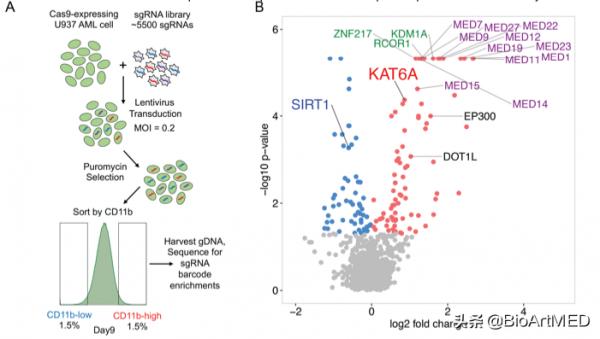
為了研究AML分化的表觀遺傳調控分子,作者設計了一個包含904個基因的sgRNA文庫,這些基因包括chromatin regulator以及一些RNA結合蛋白。作者利用U937細胞系作為篩選的細胞系,以CD11b作為篩選的marker,透過流式細胞分選篩出CD11b高低表達的細胞。經過篩選,作者在CD11b低表達的細胞中找到了56個相關基因,在高表達細胞中篩選到73個相關的基因。作者對這些基因的功能做了細緻的分類,其中一些基因為已知的被調控AML分化的基因,表明了篩選的有效性。作者發現,在CD11b高表達組中,KAT6A顯著富集;同時在低表達組中,去乙醯化酶SIRT1顯著富集。因此,作者推測KAT6A可能在AML分化中起著重要的作用。
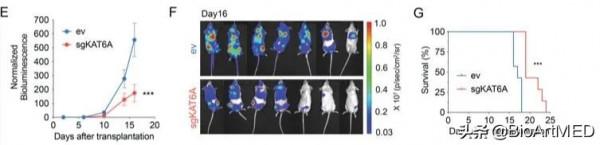
作者利用TCGA、TARGET、GTEx以及CCLE等資料庫,作者發現,KAT6A在LAML中高表達,KAT6A在AML中表達高於正常的組織。另外,KAT6A高表達的AML樣本中分化相關基因的表達都受到抑制,因此,作者推測,KAT6A抑制了AML的分化,並且在AML疾病的發生發展過程中起著重要的作用。作者進一步在細胞以及小鼠水平研究了KAT6A的功能,發現敲除KAT6A促進了AML細胞的分化;將敲除KAT6A後的AML細胞接種至小鼠後,小鼠的生存期較接種WT的AML細胞顯著延長。另外,作者驗證了KAT6A的乙醯轉移酶的酶活性對於其調控AML分化的影響,發現KAT6A的酶活性對於其調控AML分化作用時必要的。
圖2. KAT6A敲除抑制AML
作者進一步研究了KAT6A調控AML分化的分子機制, RNA-seq結果表明在敲除KAT6A後,細胞週期相關的基因以及MYC相關的基因表達水平顯著降低,而在KAT6A敲除細胞中過表達MYC後能夠部分逆轉 KAT6A敲除表型。因此,作者推測KAT6A可能透過啟用MYC等基因,從而調控了AML的分化過程。進一步的KAT6A,H3K9ac, H3K14ac, H3K23ac的ChIP-seq實驗發現,KAT6A可能透過直接促進H3K9ac從而推動了MYC, MYB, and LAMP5等基因的表達、並抑制了AML的分化。另外,作者發現ENL可以作為reader來識別H3K23ac,從而招募RNA聚合酶、促進相關基因的轉錄。
綜上,作者證實了KAT6A可以作為乙醯轉移酶促進H3K23ac,H3K23ac被ENL識別,從而促進相關基因的轉錄,並抑制AML的分化過程。進一步的研究發現,KAT6A的抑制劑WM-1119可以顯著抑制AML,因此,KAT9A抑制劑以及其與其他的藥物的聯用,可能能夠為治療AML帶來新的曙光。
原文連結:
doi:10.1158/2159-8290.CD-20-1459
製版人:十一
轉載須知