編者按:2021年乳腺癌治療領域碩果累累,新輔助治療、輔助治療、晚期治療進展不斷。《腫瘤瞭望》特邀上海交通大學附屬第一人民醫院朱麗教授與復旦大學附屬腫瘤醫院王中華教授共同對相關研究進行了回顧,以饗讀者。
01
腫瘤瞭望:隨著精準治療理念的提出及治療藥物的更新迭代,乳腺癌患者的整體生存不斷延長。請兩位教授回顧過去一年,分別就國內外早期和晚期乳腺癌談談其重要進展。
朱麗教授:作為一名外科醫生,我的確也非常關注乳腺癌新輔助方面的進展,我將按照乳腺癌的分子分型,從三個層面和大家分享近年來的一些進展。
對於三陰性乳腺癌,在新輔助治療領域中當前我們對化療的探索空間有限,但是在免疫治療中我們取得了很多進展。KEYNOTE-522研究證實,在新輔助治療階段,帕博利珠單抗聯合化療對比單純化療組能顯著提高pCR,從而成為了第一個在早期乳腺癌新輔助治療領域獲批的藥物。
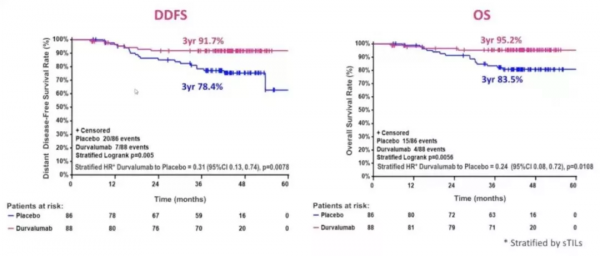
除了帕博利珠單抗外,其它藥物也取得了相應進展,也有pCR率的提高或額外的生存獲益。Ⅱ期的GeparNuevo研究雖未提高整體人群的pCR率,但是今年ASCO報道的生存資料卻顯示度伐利尤單抗組的3年DDFS率(91.7% vs 78.4%)和OS率(95.2% vs 83.5%)均有提高。雖然這項研究的主要研究終點並不是患者的生存率,在輔助治療階段也並沒有繼續使用相應的免疫治療,但它也讓我們看到了患者的生存獲益,值得我們在今後的研究中做進一步的探索。
在三陰性乳腺癌輔助治療階段,三性陰乳腺癌的標準治療仍然是化療。因此我們要重點探索化療的組合方式以及強化方案。復旦大學附屬腫瘤醫院的PATTERN研究(紫杉醇+卡鉑輔助治療)以及中山大學腫瘤防治中心的SYSUCC-001研究中一年的卡培他濱節拍輔助治療方案,均能夠給患者帶來生存獲益。這兩項中國本土的研究都登上了JAMA Oncology這一高質量的學術期刊,同時被納入了NCCN指南,這也是值得驕傲的一點。
KEYNOTE-522研究證實免疫治療能夠顯著提高新輔助治療階段的pCR率,與化療聯合安慰劑治療相比,帕博利珠單抗聯合化療組的pCR率從51.2%提升至64.8%。在輔助治療階段繼續使用一年的帕博利珠單抗能夠將患者三年的EFS率從76.8%提升到84.5%,HR=0.63,降低了37%的復發風險。從新輔助治療到輔助治療應用免疫治療,KEYNOTE-522研究給本來愈後非常差的三陰性乳腺癌患者帶來的額外生存獲益,可以說是雪中送炭。
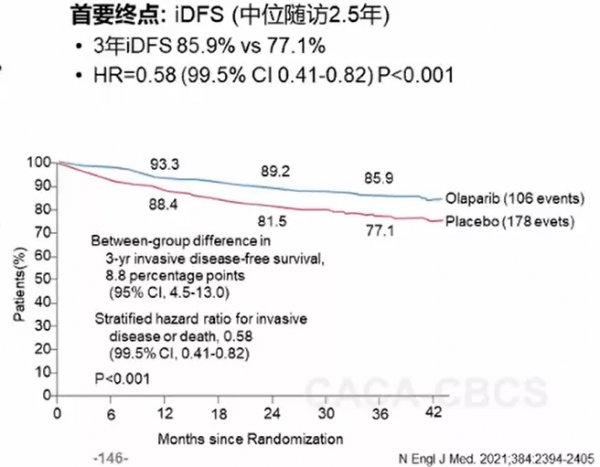
另一項重磅研究是2021年ASCO報道的OlympiA研究,該研究入組了胚系BRCA突變的HER2陰性患者,中位隨訪2.5年後進行第一次中期分析,結果顯示,奧拉帕利治療組相比安慰劑組,顯著改善3年iDFS,兩組3年iDFS:85.9% vs. 77.1%,奧拉帕利治療降低了患者浸潤性腫瘤復發或死亡風險達到42%(HR=0.58;99.5%CI:0.41~0.82;P<0.001)。3年的OS率也顯示出了獲益的趨勢,這項研究真正體現了乳腺癌的精準輔助治療。
王中華教授:晚期乳腺癌治療的目的是延長生存,控制疾病進展,所以新藥的研發仍然是從晚期患者開始的。
在晚期三陰性乳腺癌治療領域,KEYNOTE-355研究無論前期彙報的PFS,還是2021年ESMO大會彙報的OS,都改變了三陰性乳腺癌患者的治療結局。但需要強調的是,只有被定義為免疫型的晚期三陰性乳腺癌,才可能從化療聯合免疫治療中獲益。KEYNOTE-355研究入組物件為未經治療或無病生存6個月以上的晚期TNBC患者,定義的免疫型是用PD-L1 22c3免疫組化進行CPS綜合評分,結果發現,僅CPS≥10分的患者會有PFS和OS的獲益,PFS獲益從5.6個月(化療)延長到9.7個月(化療聯合免疫治療),而OS從16個月(化療)延長到23個月(化療聯合免疫治療),佔全部入組人群的38-40%。當前,化療聯合免疫治療已經成為國際三陰性乳腺癌的標準治療,但Ⅲ期的隨機研究未在中國進行,所以,我們還應在免疫治療中進行更多的探索。

KEYNOTE-355研究不同PD-L1 CPS亞組的PFS
2021年,我們中心在ASCO大會上第一次彙報了基於復旦四分型之一免疫調節型(IM型)患者的研究資料(FUTURE-C-PLUS研究),該研究用CD8標記分型,CD8細胞的免疫組織化學(IHC)評分大於10%作為IM型的cut-off值,在CD8≥10分的48例患者中,採取三藥聯合方案(卡瑞利珠單抗+白紫+法米替尼)進行治療,客觀有效率高達81.3%(95% CI:70.2%~92.3%)。2021年SABCS大會上公佈了中位隨訪17.0個月的結果,中位PFS為13.6個月(95% CI:8.4~18.8個月),12個月的OS率為82.6%(95% CI:71.6~93.6),18個月的OS率為54.4%(95% CI:36.2~72.6)。到目前為止,我們中心的接受治療的第一例患者已經應用了兩年半的藥物,仍然沒有出現疾病進展。所以免疫治療非常重要的特徵就是長拖尾效應,一旦有效,效果是非常好的。

FUTURE-C-PLUS研究2021年ASCO大會公佈的資料
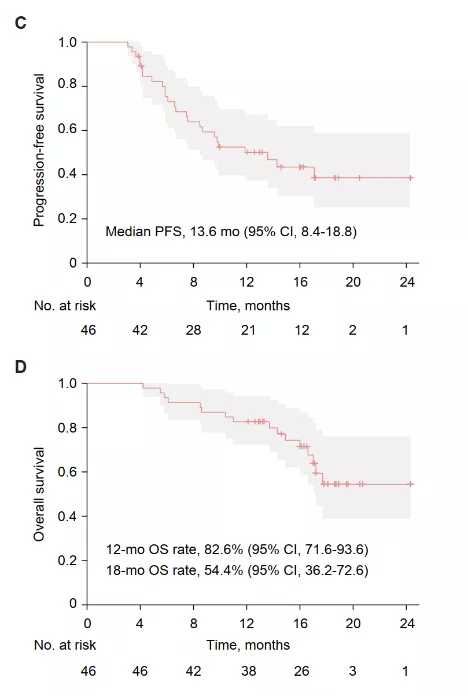
FUTURE-C-PLUS研究2021年SABCS大會公佈的資料
ADC類藥物也有效改善了晚期三陰性乳腺癌的治療療效,該類藥物也即將在中國上市,我們希望其上市能夠為晚期三陰性乳腺癌提供更多的獲益。
朱麗教授:HER2陽性乳腺癌的早期治療領域也出現了很多進展。首先介紹的是入選2021年美國聖安東尼奧乳腺癌研討會(SABCS)由復旦大學附屬腫瘤醫院吳炅教授牽頭的PHEDRA研究,該研究在新輔助治療階段使用吡咯替尼聯合曲妥珠單抗和多西他賽,pCR率為44.4%,顯著高於曲妥珠單抗聯合多西他賽組的24.3%,這項研究也在國際領域獲得了很大的成就和推廣。目前HER2陽性乳腺癌的標準新輔助治療方案是曲妥珠單抗+帕妥珠單抗的雙靶治療,PHEDRA研究由於開展時間的關係,對照組選用了單靶治療,但我們也可以從中得到一定的提示,吡咯替尼聯合曲妥珠單抗也可以給患者帶來一定的療效。
除TKI聯合大分子單抗的研究以外,還有關於大分子單抗之間化療配伍對比的研究。由廣東省人民醫院王坤教授牽頭的neoCARH研究提示豁免蒽環的可能,該研究頭對頭的比較TCH組和EC-TH組的pCR率,TCH組的pCR率(55.9% vs. 37.3%)和ORR(95.5% vs. 89.4%)均高於EC-TH組。結果提示用更少、毒性更小的藥物能夠獲得療效上的獲益,從而減少患者毒副反應,因此ASCO指南把TCbH聯合靶向治療作為優先推薦。另外,WSG-ADAPT研究也做了一些新輔助降階梯到無化療的探索。
目前曲妥珠單抗聯合帕妥珠單抗的雙靶治療已經成為晚期乳腺癌新輔助治療的一線標準方案,但是我們對低危患者的曲妥珠單抗短療程輔助治療的探索一直沒有停止過。2021年ESMO報道的一項薈萃分析顯示,6個月療程組的5年iDFS率非劣效於12個月組(89.26% vs. 88.56%,HR=1.07,非劣效P=0.02),但9周療程沒有達到非劣效(91.40% vs 89.2%,HR=1.27,非劣效P=0.56)。其實這項薈萃分析還是有一些爭議的,因為我們不能完全透過一項薈萃分析的結果來指導臨床,而需要看納入的原文,分析為什麼會有這樣的結果。所以我們對於減療程的考慮還是要慎重,畢竟不是所有的臨床試驗都顯示了這樣的結果。
在考慮降階梯治療的同時,我們也要考慮哪些患者要進行升階梯治療。ExteNET研究顯示,早期乳腺癌患者接受奈拉替尼的延長輔助治療能夠顯著改善DFS和OS。值得注意的是,ExteNET研究開展年限比較早,入組的患者均接受的是單靶治療。而目前的高危患者會在新輔助治療階段使用曲帕雙靶治療,如果新輔助治療沒有達到pCR,我們會按照KATHERINE研究的模式強化使用T-DM1。但是ExteNET研究並沒有回答TKI能否改善這部分患者的生存。2021年St.Gallen會議針對是否選擇用TKI進行強化進行了一次投票,超過一半的專家推薦對淋巴結大於4枚,新輔助治療階段沒有達到pCR的高危患者採用奈拉替尼強化。臨床實踐中,我們每位醫生也會根據每個病人的具體情況進行相應的治療推薦。以上就是我對輔助治療的一點體會和心得。
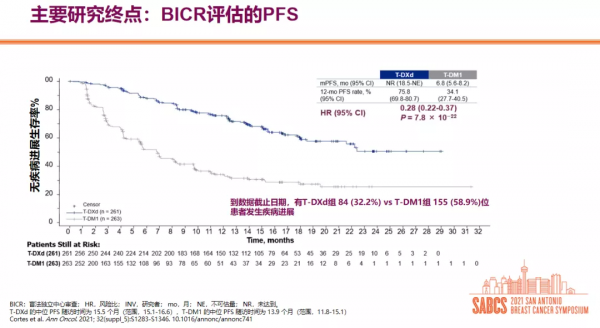
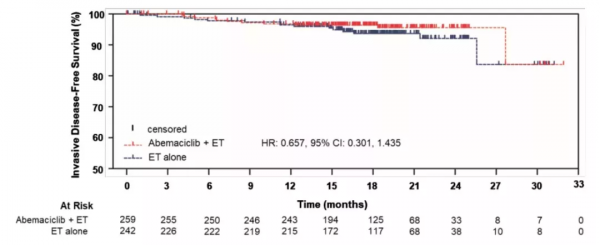
王中華教授:在HER2+乳腺癌的治療中,2021年最重要研究的是DESTINY-Breast 03研究,這是第一個直接頭對頭比較兩種ADC藥物的Ⅲ期臨床試驗。2021年ESMO資料顯示,T-DXd組PFS顯著優於T-DM1組(25.1 vs. 7.2個月),OS有優效性趨勢(12個月OS率94.1% vs. 85.9%),ORR(79.7% vs. 34.2%),且各亞組獲益趨勢一致。基於此,T-DXd已經成為NCCN指南HER2+晚期乳腺癌患者二線治療的優選方案,改變了晚期HER2陽性二線治療的標準。
2021年ESMO大會公佈的DESTINY-Breast 03研究PFS結果
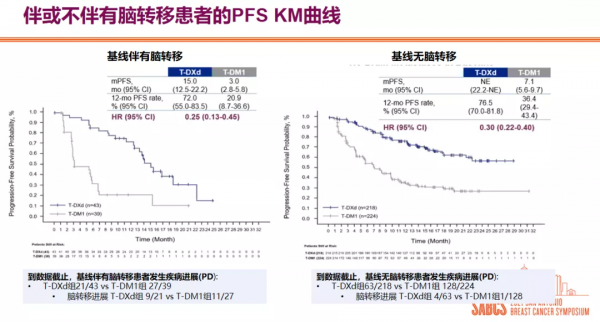
2021年SABCS大會上,DESTINY-Breast 03研究資料再次進行了更新,結果顯示,T-DXd治療方案相比T-DM1在各亞組都展現出持續的療效獲益,且無論患者伴或不伴有腦轉移,T-DXd對比T-DM1都表現出了更佳的療效,T-DXd治療也可以帶來潛在的顱內緩解和減輕中樞神經系統(CNS)疾病。
2021年SABCS大會公佈的DESTINY-Breast 03研究結果
III期臨床試驗DESTINY-Breast09研究已經啟動,該研究是一項全球頭對頭的III期臨床試驗,旨在評估T-DXd聯用或不聯用帕妥珠單抗與標準治療(THP:紫杉烷、曲妥珠單抗和帕妥珠單抗)相比一線治療HER2陽性轉移性乳腺的安全性和療效。這是首個評估T-DXd用於一線治療HER2陽性轉移性乳腺癌臨床研究。因此,我們也希望該研究能帶來更多好訊息,從而為患者帶來更多獲益。
朱麗教授:最後談談在Luminal型乳腺癌患者的內分泌治療領域的更新。通常新輔助內分泌單藥用藥在兩週左右,Ki67的變化能夠提示患者的生存療效,這是ADAPT系列研究得到的啟示。目前AI/TAM聯合CDK4/6抑制劑的研究也在進行中,我們期待內分泌治療能在Luminal型乳腺癌患者中為我們帶來更多進展。
Ⅲ期monarchE研究首次證實對於高危乳腺癌患者,應用CDK4/6抑制劑輔助治療可以顯著地改善患者生存的臨床研究,2021年ASCO大會上報道了中國亞組患者的資料,和全球患者獲益一致。兩年的隨訪時間不是很長,但是iDFS率已經能從92.1%提升到95.6%,因此,CDK4/6抑制劑被獲批用於HR+/HER2-乳腺癌的輔助強化治療。
既往對於高危的患者我們採用內分泌延長治療的策略,或對絕經前的患者使用OFS來做內分泌強化,現在我們從內分泌耐藥的機制上,把CDK4/6抑制劑更早的結合在輔助治療階段,進一步改善了這部分高危患者的愈後。
王中華教授:對於HR+/HER2-晚期乳腺癌患者的治療,當前CDK4/6抑制劑的地位已經確立,2021年MONALEESA-2、MONALEESA-3、PALOMA-3等生存資料,也顯示了持續的生存獲益。徐兵河教授領導的DAWNA-1研究中結果的公佈,使我們看到了國產原研的Dalpiciclib+氟維司群用於二線治療也可顯著改善患者PFS(15.7 vs. 7.2個月,HR=0.42)。此外,對於具有高復發風險且Ki-67≥20%的早期乳腺癌患者的輔助治療,CDK4/6抑制劑聯合內分泌治療方案也以獲批。
關於PI3K/Akt/mTOR通路,2021年ESMO大會報道的針對中國患者的BOLERO-5研究取得了與BOLERO-2一致的結果,依維莫司+依西美坦用於AI進展的絕經後患者,可相較於安慰劑組顯著延長中國患者PFS(7.4個月vs2.0個月,HR0.52);徐兵河教授領導的MIRACLE研究也發表在JAMA腫瘤學雜誌,依維莫司+來曲唑用於TAM失敗患者,同樣可顯著延長PFS(19.2 vs 11.0個月)。
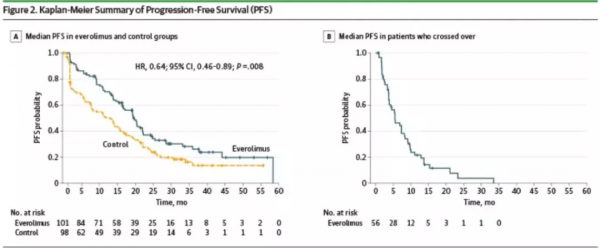
MIRACLE研究中ITT人群(A)和交叉人群(B)的PFS K-M曲線
以上就是我對近年來乳腺癌新輔助治療領域進展的回顧。
02
腫瘤瞭望:正如本次會議的主題——“譜新章、得芳華”,我們希望透過不斷創新的治療方案,為患者贏得更多治療希望。展望未來,您認為有哪些研究可能會進一步為乳腺癌的實踐帶來變革?
王中華教授:我們相信今後會有一系列的臨床研究能夠為晚期三陰性乳腺癌患者帶來更多獲益。復旦分型對於三陰性乳腺癌的治療也有一系列的佈局,現在FUTURE系列研究已經佈局到患者的第四、五線治療。我們非常期待的就是在一線治療中,在四分型的基礎上聯合不同的靶向治療藥物,對比傳統的白蛋白紫杉醇化療的結果,目前研究入組已經接近尾聲。希望今後在三陰性乳腺癌的一線治療中有更多的突破。也感謝邵志敏教授團隊提供了非常好的基礎研究資料,能為晚期三陰性乳腺癌後續治療帶來更多的希望。